免洗消毒凝胶企业标准备案如何办理 什么是“三新”消毒产品 如何申请“三新”消毒产品卫生行政许可
免洗消毒凝胶企业标预备案如何操持
在很多时分我们在停止执行规范央求的时分我们都需求停止交钱才干停止央求,那么停止这种央求需求哪些步骤流程呢?多少钱才干停止央求呢?下面就有小编为大家处置一下相关知识吧,希望可以协助到大家!
企业产品规范是企业组织消费和交货的依据,也是监视反省的依据。《〈中华人民共和国规范化法〉方法》第三条规则,企业应执行规范化法律、法规,严厉按规范组织消费和经销,制止无规范消费。《中华人民共和国规范化法》第六条规则,企业消费的产品没有国度规范和行业规范的,应当制定企业规范,作为组织消费的依据。企业的产品规范须报外地府规范化行政主管部门和有关行政主管部门备案。已有国度规范或许行业规范的,国度鼓舞企业制定严于国度规范或许行业规范的企业规范,在企业外部适用。
那么企业规范怎样做才干表现自己产品的优势呢?
已有国度规范或许行业规范的,国度鼓舞企业制定严于国度规范或许行业规范的企业规范,在企业外部适用。指定高于国度国度或许行业的企业规范可以提升产品的价值和企业的笼统,由于企业执行高于国度规范和行业规范和消费规范,是对自己企业严厉要求,对产质量量严厉要求以及对广阔消费者群众担任的表现。而且更能提升产品的市场价值,所以企业标预备案是值得做的,而且是上市前必需要做的
企业标预备案操持流程
首先依据产品的特性,用途,材质等编制企业规范说明,然后需求请专家团审批,专家团有5位组成,会针对您制定的企业规范停止休会评审,编写会议纪要,*后专家签字,到此,企业规范的编写就完成了,然后到质检局完成*后一步备案,那么如今有办公的多元化和拇指化呢,国度也是相机守旧了网上备案,企业公共信息效劳平台,只需完成前面的步骤,备案直接在网上停止公示就好。
执行规范操持流程多久费用多少
(一)执法依据 《中华人民共和国规范化法》、《XX省规范化管理方法》
(二)受理范围 凡在本区域内从事消费并用于销售的产品在尚无国度规范、行业规范或中央规范的状况下,应由企业制定相应的企业规范,作为企业组织消费和判定产质量量的依据。企业规范须报外地府规范化行政主管部门备案。
(三)企业标预备案手续 1.企业规范应在规范同意发布后30日内,按企业附属关系到外地质量技术监视局备案。市属和开发区企业到XX市质量技术监视局规范化科备案。委托加工企业,由委托方到外地质量技术监视局操持备案手续。 2.企业标预备案时,应提供以下资料: (1)规范文本;(2)编制说明;(3)备案表;(4)审定纪要;(5)审定人员名单;(6)有效的营业执照或注销证书复印件(*);组织机构代码证书复印件及电子正本。 上述资料1-5项一式两份。
3.提交资料的要求 (1)规范文本 企业规范文本格式应契合GB/T1.1-2000和GB/T1.2-2002规则要求。规范文本格式包括:规范封面、前言、 首页、中间页和末页。其中封面右上角Q/**中的**为各县郊区局、集团公司、总公司的代号。 企业规范编号按下述规则执行。
1)企业规范代号Q/代表企业制定、同意、发布的企业规范。
2)企业附属行政区域代号是用县(市)、区称号或工业局、总公司称号的二位汉语拼音字头表示。
3)企业代号由企业定,普通用企业称号的汉语拼音字头或英文缩写的三个字母表示。如金吉利制衣有限公司代号是JJL。
4)顺序号是企业自己制定的企业规范号,用三位阿拉伯数字表示。如:001。
5)年代号为规范发布的年代,用四位数表示。如2005。
(2)编制说明 企业规范编制说明普通包括以下内容: 1)义务来源,制定该规范的目的和意义,任务简明进程。其中包括:调研、实验、验证、起草进程等。 2)采用和自创国际外规范资料的状况,包括国际外规范水平剖析。 3)规范主要内容的解释,修订规范时应有新旧内容的对比,同时还要写出修订的理由。 4)贯彻该规范的措施、要求、建议。 5)技术经济效果剖析及其他应说明的效果。
(3)备案表 企业标预备案前,企业须填写《XX县市企业标预备案表》,《XX县市企业标预备案表》由企业法人代表或其授权的企业主管指导审批赞同,加盖企业公章。
(4)审定纪要 企业规范审定纪要普通包括以下内容: 1)企业规范审定会时间、地点、参会人员、掌管人等。 2)讨论中严重效果的分歧修正意见,普通效果的准绳修正意见。 3)对规范起草单位的要求,如修正进度、修正方法以及修正后能否需求再停止审定。 4)审定结论性意见,即完全经过,还是基本经过,还是没经过。
(5)审定人员名单 企业规范审定会由企业组织,审定人员要求大专以上学历,有一定专业知识。审定人员可以是本单位的技术人员,也可外聘专家,总人数不得少于5人。审定人员应在审定人员名单上签字。
4.受理机关应在十个任务日内对企业提供的资料停止复核,契合《XX市企业标预备案规则》的企业规范即予以备案,并在《XX市企业标预备案表》和企业规范文本封面上加盖备案公用章。不契合《XX省企业标预备案规则》的,退还企业并一次性书面告之理由。
(四)企业规范的修正和复审 1.经备案的企业规范如有修正或补充的,应由企业填写《企业规范修正通知单》一式三份,到原备案机关操持修正或补充手续。备案部门应在原备案的规范文本上注明修正日期。已采用国际规范的,修正时不得降低其规范水平。
2.企业规范应活期复审,复审周期不得超三年。当新的国度规范、行业规范或中央规范发布时,企业规范必需及时复审。企业规范复审时,应由企业填写《企业规范复审结果通知单》一式三份,到原备案机关操持确认继续有效或废止手续。经复审,被确认有效的企业规范,备案机关应在原备案的规范文本上盖章注明白认日期。确认后的企业规范,原规范编号继续有效。经复审,被以为需求重新修订的企业规范,应予以废止。废止的企业规范,由备案机关加盖规范注销印章。重新修订的企业规范,应到备案机关重新操持备案手续。
免洗消毒凝胶企业标预备案如何操持 什么是“三新”消毒产品?如何央求“三新”消毒产品卫生行政容许 健明迪检测
检测认证行业8年:*类、第二类消毒产品应依照《国度卫生计生委关于印发消毒产品卫生平安评价规则的通知》(国卫监视发〔2014〕36号)及《消毒产品...什么是“三新”消毒产品?如何央求“三新”消毒产品卫生行政容许
后疫情时代背景下,消毒产品的运用率大大提高,运用场景颇多,产品类型多种多样,企业在传统的消毒产品基础上开发研制新产品也成为趋向。关于中国“三新”消毒产品卫生行政容许央求。
何为“三新”消毒产品?
“三新”消毒产品是指应用新资料、新工艺技术和新杀菌原理消费消毒剂和消毒器械,其有效性、平安性、环境顺应性等方面应当较惯例产品具有同等功用或愈加完善。
新资料需应同时满足下列条件:
- 未列入消毒剂原料有效成分清单(表1)的;
- 未列入《中华人民共和国药典》中消毒防腐类的;
- 未列入现行国度卫生规范、规范的。
新工艺技术:指消费技术参数和/或工艺流程的改动,招致消毒剂和消毒器械的有效性、平安性和环境顺应性同等或优于惯例产品的消费加工技术。
新杀菌原理:指未列入消毒因子及其相应消毒器械清单、指示物清单(表2、表3)的,以物理、化学、生物消毒因子或相互协同作用发生的杀菌原理及其指示物。
“三新”消毒产品卫生行政容许央求大致流程
依据《新消毒产品受理规则》,新消毒产品的申报流程汇总如下:
- 先登录卫生监视中心网上申报系统(点击申报)停止行网上申报;
- 向卫健委提交书面央求资料及样品,国度卫生计生委设立新消毒产品评审委员会,承当新消毒产品技术评审任务;
- 卫健委依据评审委员会的技术评审结论停止行政审查,作出能否同意的决议;
- 卫健委给出过补正意见的,央求人应当在1年内依照《央求资料补正通知书》要求提交补正资料、补充资料,逾期未提交的,视为自动坚持。
基于瑞旭集团日化事业部临时从事着中国消毒产品卫生平安评价和备案任务的阅历,市场上罕见的消毒产品类型大多为手消毒剂、物表消毒剂、空气消毒剂、抗抑菌制剂等,目前在全国消毒产品网上备案信息效劳平台上也有几万余款消毒产品停止了备案,包括*类消毒产品和第二类消毒产品。在这些已有消毒产品基础上,人类为了顺应经济开展形成的日益破坏的自然环境,企业为了寻求更久远的开展,“三新”消毒产品肯定成为一种开展趋向。因此“三新”消毒产品法规完善指日可待。
“三新”消毒产品受理信息
经过国度卫健委官方网(点击查询)查询可知,自2014年至今,共受理了25款新消毒产品的央求,其中2020年疫情迸发后受理的产品数目*多,2020年至今共受理了23款新消毒产品央求,到达总受理量的90%以上,但目前没有任何一款“三新”消毒产品被予以经过,已受理的新消毒产品详细信息如下(表1):
表1 2014年至今“三新”消毒产品受理信息
转载自:妆合规 作者:瑞旭集团
免洗消毒凝胶企业标预备案如何操持 什么是“三新”消毒产品?如何央求“三新”消毒产品卫生行政容许 健明迪检测
消字号/消毒产品备案合规要求清点!
◆ 注释 ◆
5月7日,为助力企业合规消费、销售及进出口消毒产品,日化*前线约请到杭州瑞旭集团(CIRS)农药和消毒产品法规事业部经理——唐艳霞女士,停止了《消毒产品合规要求清点》的线上直播分享,小助手特整理了本场直播的精彩内容,下面我们一同回忆关于消毒产品合规要求方面的信息。
01消毒产品消费及原料法规要求
▶ 什么是消毒产品?
产品定义:指专门用于杀灭和肃清传达媒介上的病原微生物,以化学、物理或生物方式预防控制感染性疾病或传染性疾病的一类特殊的安康相关产品。
作用方式:化学、物理、生物方式杀灭或肃清病原微生物。
运用场所:人体外部环境:医疗器械、皮肤、黏膜、餐饮具、瓜果蔬菜、水、环境、物体外表、空气、污物等。
防治对象:病原微生物,包括金黄色葡萄球菌、大肠杆菌、白色念珠菌、铜绿假单胞菌、细菌芽胞、龟分枝杆菌、白色葡萄球菌、黑曲霉菌、脊髓灰质炎病毒等。
▶ 消毒产品分类
产品类别:
• 消毒剂(含氯消毒剂、过氧化物类消毒剂、醛类消毒剂、醇类消毒剂、含碘消毒剂、酚类消毒剂、环氧乙烷、双胍类消毒剂和季铵盐类消毒剂);
• 消毒器械(包括生物指示剂、化学指示剂及灭菌包装物);
• 卫生用品(一次性卫生用品+抗抑菌制剂)。
风险等级:
• 第 I 类:较高风险,需严厉管理以保证平安、有效的消毒产品(包括用于医疗器械的高水平消毒剂和消毒器械、灭菌剂和灭菌器械,皮肤、黏膜消毒剂,生物指示物、灭菌效果化学指示物等);
• 第 II 类:中度风险,需求增强管理以保证平安、有效的消毒产品(包括除*类产品外的消毒剂、消毒器械、化学指示物,以及带有灭菌标识的灭菌物品包装物、抗(抑)菌制剂等);
• 第 III 类:风险水平较低,实行惯例管理可以保证平安、有效的除抗(抑)菌制剂外的卫生用品(是除抗(抑)菌制剂外的卫生用品,如妇女经期卫生用品、尿布等排泄物卫生用品、其他的一次性卫生用品等)。
▶ 消毒产品监管法规体系
▶ 消毒产品消费要求
·卫生消费容许:
在国际从事消毒产品消费、分装的单位和团体,必需依照相关规则要求申领消毒产品消费企业卫生容许证一企终身产场所一证,一个集团或公司拥有多个消费场所的,应区分央求卫生许证。
消毒产品消费企业卫生消费容许证
·平安消费容许:
企业消费列入《风险化学品目录》 中的消毒产品成品或许中间产品, 还应依照规则规则取得风险化学品平安消费容许证。
风险化学品平安消费容许证
▶ 消毒产品消费企业的卫生监视内容
外地卫生监视部门或机构主要抵消毒产品消费企业停止以下卫生监视:
• 消毒产品及消费企业卫生容许资质;
• 消费条件(消费皮肤黏膜消毒剂&抗抑菌制剂&卫生用品需求污染车间、消费戊二醛车间需通风设备、消费乙醇车间需防爆设备),消费进程(能否执行规范操作规程和管理制度,能否添加国度规则禁用的物质);
• 运用原资料卫生质量;
• 消毒产品和物料仓储条件;
• 消毒产品从业人员装备和管理状况;
• 消毒产品卫生质量:出厂检验;
• 卫生平安评价报告+说明书标签。
▶ GB 38850-2020 规范解读
2020年4月9日,国度市场监视管理总局及中国国度规范化管理委员会发布GB 38850-2020《消毒剂原料清单及禁限用物质》,规则了运用于不同消毒对象消毒剂的原料成分清单和运用范围,同时规则了消毒剂配方中的禁用和限用成分。
• 活性成分原料
• 惰性成分原料
惰性成分概念:指在消毒剂配方中,具有防腐蚀、护肤、动摇、调停酸碱度、调味和着色等辅佐作用的物质。
惰性成分清单:消毒剂产品仅可运用清单中规则的115种惰性原料,除破损皮肤和黏膜外,其他用途的消毒剂的着色剂和香料也可参照食品添加剂或许化装品的相关要求。
惰性成分运用范围:每种惰性成分都有规则的运用范围,不可超范围运用。
• 禁限用物质
仅对皮肤消毒剂和黏膜消毒剂中的局部原料成分停止了限量规则,与之前规范中禁限用要求区别不大。
02消毒产品卫生平安评价及标签宣称要求
▶ 消毒产品卫生平安评价
产品责任单位在*类和第二类(消毒剂、消毒器械、抗抑菌制剂)消毒产品初次上市前对产品有效性和卫生平安性停止综合评价,构成《消毒产品卫生平安评价报告》,并对评价结果担任,可将有关卫生平安评价报告录入全国信息效劳平台停止备案。
参考法规:
平安评价:WS 628-2018《消毒产品卫生平安评价技术要求》与《消毒产品卫生平安评价规则》(2014版)配套运用;
检测:《消毒技术规范》2002版、产品卫生规范。
▶ 评价&备案资料要求
消毒产品卫生平安评价备案,需预备以下资料:
• 封面;
• 备案注销表、平安评价基本状况表;
• 市售标签(铭牌)、市售说明书;
• 检验报告(含结论);
• 国产产品备案企业规范或出口产质量量规范;
• 国产产品消费企业卫生容许证;
• 出口产品消费国(地域)允许消费销售的证明文件(公证)及报关单;
• 出口产品在华责任单位授权书(公证);
• 消毒剂、抗(抑)菌制剂产品配方;
• 消毒器械元器件、结构图;
• 其他(产品照片、委托加工合同、商标文件等)。
▶ 检测要求(有CMA资质)
▶ 消毒产品平安评价&备案流程
▶ 《消毒产品标签说明书管理规范》
适用对象:适用于在中国境内消费、运营或运用的出口和国产消毒产品;
基本要求:应当真实,不得有虚伪夸张,不得有明示或暗示对疾病的治疗作用和效果的内容(抗抑菌制剂);
产品标识和称号:应采用中文标识;产品称号应契合 《卫生部安康相关产品命名规则》,包括商标名(或品牌名)、通用名、属性名;
未列入消毒产品分类目录的产品不得标注任何与消毒产品管理有关的卫生容许证明编号(如消毒湿巾)。
消毒产品标签标注内容:
消毒产品标签制止标注内容:
03消毒产品进出口法规要求
▶ 属于风险化学品、风险货物的消毒剂
• 醇类消毒产品(乙醇(体积比>24%)消毒凝胶、异丙醇消毒液、酒精湿巾);
• 氧化剂类消毒产品(含有次氯酸钠、次氯酸的消毒产品、过氧乙酸(含量>8%));• 季铵盐类消毒剂(高浓度季铵盐(含量>5%)风险货物);
• 复合碘产品。
▶ 法律法规
▶ 消毒产品出口要求
• 确定产品在华责任单位;
• 停止卫生平安评价&备案(I类、II类消毒产品),检测(III类消毒产品);
• 契合消毒产品标签,SDS和GHS标签;
• 确定HS code(380894项下);
• 按要求提供报检资料;
• 出口商停止风险化学品注销、风险化学品运营容许证;
• 国际运输合规。
▶ 消毒产品出口要求
▶ 进出口报检资料
• 出口风险化学品运营企业契合性声明;
• 出口风险化学品消费企业契合性声明;
• 《出境风险货物包装容器功用检验结果单》(散装货物除外);
• 风险特性分类鉴别报告;
• 中文平安数据单、中文风险公示标签样本;
• 对需求添加抑制剂或动摇剂的产品,应提供实践添加抑制剂或动摇剂的称号、数量等状况说明;
• 出口属于风险货物的消毒剂的消费企业还应向所在地海关央求出口风险货物包装运用鉴定。
04消毒产品运输要求引见
▶ 风险货物在中国的运输
风险货物在中国运输,如采用不同的运输方式,依照不同的规范执行。
▶ 大批风险化学品在中国运输
“风险化学品”制止普通快递运输:
依据风险化学品平安管理条例-2011,第六十四条:任何单位和团体不得交寄风险化学品或许在邮件、快件内夹带风险化学品,不得将风险化学品匿报或许谎报为普通物品交寄。邮政企业、快递企业不得收寄风险化学品。
例外数量(EQ)&有限数量(LQ):是指风险货物在移交运输时,如数量较少,且包装满足一定要求,即可免除运输时的局部合规要求(例如,承运人资质,包装功用测试)。
参考法规:GB28644.1-2012 风险货物例外数量和包装要求;GB28644.2-2012 风险货物有限数量和包装要求;风险货物路途运输平安管理方法。
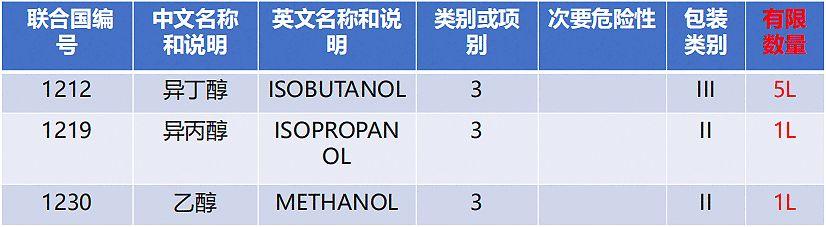
▶ 风险货物–例外数量和有限数量运输
风险货物必需是包装类Ⅱ或Ⅲ;包装类Ⅰ的风险货物不得限量;必需应用组合包装(内包装置于外包装之内)。
限量的准绳是把大包件分解成小包件,然后将小包件置于外包装内。双层包装维护产品和能够的小渗漏。包括:吸附资料、衬垫等维护内容器的部件。